Badanie EuroPainClinics® Study II
Celem projektu EPCS II jest porównanie stanu klinicznego pacjentów, którzy po spełnieniu kryteriów wskazań poddali się zabiegowi w zakresie epiduroskopii.
Badanie EuroPainClinics®Study II (EPCS II) obiektywizuje wkład małoinwazyjnego zabiegu algezjologicznego – epiduroskopii u pacjentów z bólem pleców, którzy poddali się jednej lub kilku nieskutecznym operacjom kręgosłupa i dolega im tzw. zespół bólowy po nieskutecznych operacjach kręgosłupa (failed back surgery syndrom – FBSS). Badanie skupia się na obserwacji długotrwałej ulgi w bólu i poprawy jakości życia takich pacjentów.
Dnia 23.4.2015 r. badanie zostało zatwierdzone przez regionalną szpitalną komisję etyczną pod numerem EK:75/EK/15. Następnie zostało zarejestrowane w międzynarodowej bazie danych National Health Service USA. https://clinicaltrials.gov PRS: NCT02459392.
 EPCS 2 Approval document
EPCS 2 Approval document
Projekt spełnia wszystkie atrybuty i wiążące normy prawne dotyczące zabiegu medycznego zatwierdzonego przez Ministerstwo Zdrowia w Republice Słowackiej i Czeskiej.
Szczegóły badania
Badanie Europainclinics®Study II (EPCS II) obiektywizuje wkład małoinwazyjnego zabiegu algezjologicznego – epiduroskopii.
Zabieg w zakresie epiduroskopii – kryteria wskazań
Badanie Europainclinics®Study II (EPCS II) obiektywizuje wkład małoinwazyjnego zabiegu algezjologicznego – epiduroskopii u pacjentów z bólem pleców, którzy poddali się jednej lub kilku nieskutecznym operacjom kręgosłupa i dolega im tzw. zespół bólowy po nieskutecznych operacjach kręgosłupa (failed back surgery syndrom – FBSS). Badanie skupia się na obserwacji długotrwałej ulgi w bólu i poprawy jakości życia takich pacjentów.
Przedmiot badania EPCS II i rejestracja
Przedmiotem projektu jest realizacja wieloośrodkowego randomizowanego badania klinicznego z podwójnie ślepą próbą zajmującego się porównaniem dwóch procesów metodycznych wykonania zabiegu w zakresie epiduroskopii u pacjentów z FBSS.
Badanie zostało przygotowane i wypracowane przez organizację Europainclinics z.ú. Po wypracowaniu projektu badania, przygotowaniu świadomych zgód dla jego uczestników i wykonaniu protokołu badanie dnia 23.4.2015 r. zostało zatwierdzone przez regionalną szpitalną komisję etyczną pod numerem EK: 75/EK/15)Następnie zostało zarejestrowane w międzynarodowej bazie danych National Health Service USA https://clinicaltrials.gov PRS: NCT02459392.
Projekt spełnia wszystkie atrybuty i wiążące normy prawne dotyczące zabiegu medycznego zatwierdzonego przez Ministerstwo Zdrowia w Republice Słowackiej i Czeskiej. Przetwarzanie danych osobowych pacjentów w celu przeprowadzenia badania wykonywane jest w zgodzie ze współczesną wersją Deklaracji Helsińskiej z 2008 r. i jednocześnie w zgodzie ze stosownymi ustawami danego kraju. Ochrona danych osobowych pacjentów zostanie zachowana. Dane będą przetwarzane według wymogów dyrektyw UE: dyrektywa 95/46/WE, dyrektywa 2002/58/WE, dyrektywa 2006/24/WE. Zostanie zapewnione, żeby protokół badania, świadome zgody z zabiegiem interwencyjnym i z odbywającym się badaniem zostały według miejscowych wymogów przedstawione stosownej niezależnej komisji etycznej. Jeżeli wymagają tego ustawy danego kraju, organizacja EuroPainClinics z.ú. poniesie odpowiedzialność za coroczne przedstawienie aktualizacji dokumentacji niezależnej komisji etycznej. Wyniki osiągnięte w badaniu zostaną opublikowane w międzynarodowych periodykach specjalistycznych i uwzględnione w poleceniach i procedurach dla praktyki klinicznej algezjologii interwencyjnej.
Przebieg badania EPCS II
Celem projektu będzie porównanie dwóch grup pacjentów, którzy poddają się zabiegowi w zakresie epiduroskopii. W grupie pacjentów A podczas epiduroskopii będzie wykonana tylko liza mechaniczna zrostów włóknistych. W grupie pacjentów B razem z lizą mechaniczną adhezji będzie wykonana aplikacja kortykosteroidów – depo-medrolu i hialuronidazy. Podczas adhezjolizy lekarz celowo pod kontrolą wizualną rozbije zrosty, które uciskają na uszkodzony nerw lub oponę twardą. Mogą być usunięte mechanicznie – zerwaniem za pomocą szpicy naprowadzanego wizualnie epiduroskopu lub ciśnieniem przez wypłukiwanie roztworem fizjologicznym. Do zaawansowanych metod mechanicznego rozbijana zrostów należy liza laserem i pulsacyjną ablacją falami radiowymi. Podawane miejscowo lekarstwa podczas zabiegu do przestrzeni nadtwardówkowej i ich przewidywany efekt: hialuronidaza może mieć udział w rozbijaniu zrostów przez mechanizm rozszczepienia enzymatycznego. W przypadku depo-medrolu przewidywane jest jego działanie przeciwzapalne w miejscu aplikacji i następna tendencja do redukcji odpowiedzi zapalnej, migracji komórek, obrzęku, bólu i tworzenia zrostów. Bez względu na te teoretyczne założenia oddziaływania podawanych lekarstw ich wkład po dzień dzisiejszy nie został w wynikach publikowanych badań podany do weryfikacji i z tego powodu podawanie tych lekarstw uważane jest za dyskusyjne.
Cele badania EPCS II i obserwowane parametry
Celem projektu jest porównanie stanu klinicznego pacjentów, którzy po spełnieniu kryteriów wskazań poddali się zabiegowi w zakresie epiduroskopii i zostali przydzieleni do badania EPCS II. Obserwowane parametry będą wykorzystane do porównywania stanu klinicznego, wizualnego zakresu bólu, ogólnego wyniku na skali bólu, szerzenia bólu w odpowiednich dermatomach, obniżenia zużycia analgetyków oraz kwestionariusza Oswestry (oceniającego jakość życia pacjentów z bólem odcinka lędźwiowo-krzyżowego kręgosłupa). Obserwowane parametry będą odnotowywane w trzech przedziałach czasowych – przed zabiegiem (pierwsze badanie lekarskie), następnie 6 miesięcy po zabiegu (drugie badanie lekarskie) i ostatecznie 12 miesięcy po zabiegu (trzecie badanie lekarskie). Następnie wynika będą poddane analizie statystycznej. Kolejny cel projektu to opublikowanie wyników w międzynarodowych periodykach specjalistycznych.
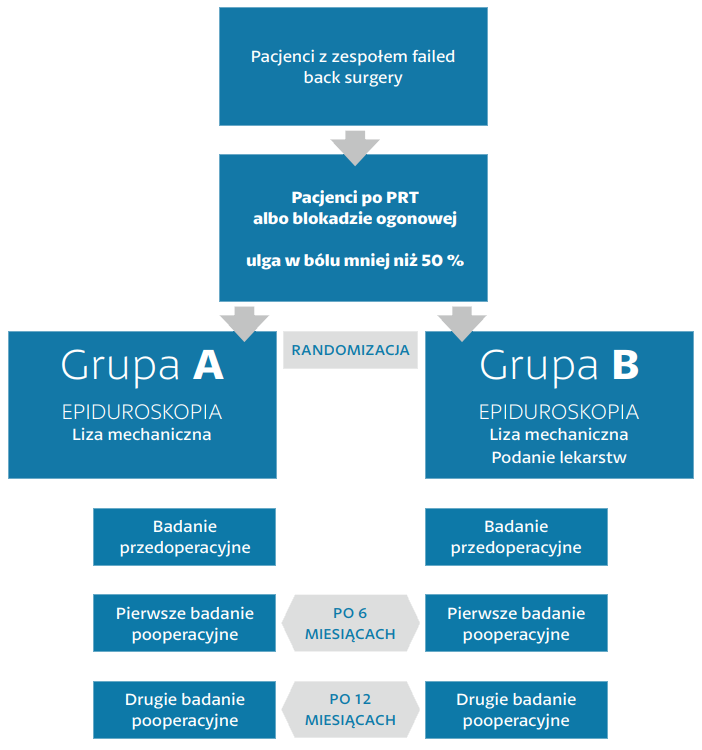
Diagram Badania EuroPainClinics®Study II
